O ciclo do nitrogênio (N) no sistema solo-planta é bastante dinâmico e complexo, uma vez que:
- O N é naturalmente encontrado no ambiente em grande diversidade de compostos químicos;
- Apresenta múltiplas transformações no sistema solo-planta
- É dependente da ação de microrganismos.
A maior fração do N do solo está na forma orgânica, presente na matéria orgânica ou como parte dos organismos vivos do solo.
A entrada do N no sistema pode ocorrer por deposição atmosférica, fixação biológica e através das adubações.
No sistema solo-planta, o N pode sofrer uma série de transformações como mineralização (amonificação e nitrificação), imobilização e desnitrificação.
Por outro lado, pode sair do sistema através da remoção pelas culturas, e por uma série de perdas que incluem: a lixiviação, a volatilização e perdas gasosas pela parte aérea das plantas, além de perdas por erosão.
Por todos esses motivos, o ciclo do N é controlado por fatores físicos e biológicos e afetado por condições climáticas difíceis de prever e controlar (Figura 1).

Etapas do ciclo do nitrogênio: dinâmica do N no solo
O N-orgânico, complexado na matéria orgânica do solo pode representar cerca de 95% do N total do solo; por isso é natural que a disponibilidade do elemento às plantas seja baixa.
Ácidos nucléicos, bases nitrogenadas, proteínas, pepetídeos, ureia, quitina, quitioses e peptideoglicano são exemplos de formas conhecidas de como o N-orgânico se encontra na natureza.
Entretanto, grande parte do N-orgânico se encontra em formas complexas, muitas delas desconhecidas, sendo apenas uma pequena parte desse material mineralizado.
Do N-orgânico total encontrado nos solos, cerca de 2 a 5% são mineralizados por ano, mas de acordo com o tipo de solo e condições ambientais este valor pode representar o suficiente no suprimento exigido pelas culturas agrícolas.
Mineralização do nitrogênio: amonificação e nitrificação
A disponibilidade do N-orgânico do solo para as plantas depende do processo de mineralização, que é definido como a conversão de compostos orgânicos nitrogenados em formas inorgânicas de N (N-NH4+ e N-NO3–).
Ocorre quando há baixa relação C/N do resíduo vegetal adicionado no solo, em condições de temperaturas adequadas e é realizado por microorganismos heterotróficos do solo, que utilizam os compostos orgânicos como fonte de energia.
Devido à elevada heterogeneidade da matéria orgânica e dos resíduos culturais a mineralização é realizada por um grupo variado de microorganismos, sendo que alguns destes são altamente especializados e só agem sobre determinados substratos.
A mineralização do N orgânico geralmente resulta em diminuição do pH do meio graças a maior liberação de prótons (nitrificação) em detrimento ao consumo (amonificação).
As condições ótimas para a mineralização do N orgânico são aquelas que favorecem a atividade microbiana:
- pH de 6 a 7,
- condições aeróbicas,
- umidade em torno de 50 a 70% da capacidade de retenção de água pelo solo,
- temperatura entre 40 e 60°C.
- baixa relação C/N (até no máximo 25 a 30/1)
- contenham baixo teor de lignina e polifenóis na sua composição.
A mineralização do N orgânico é estimulada pela adição de material orgânico fresco, rico em energia, ou de fertilizantes nitrogenados.
A mineralização do N ocorre através de dois processos: a amonificação e nitrificação. Vejamos cada um deles:
- Amonificação (N orgânico —> NH4+)
A amonificação, muitas vezes conhecida como mineralização de N, é o processo de conversão de N-orgânico nas formas amônio (NH4+) e/ou amônia (NH3).
Esta transformação ocorre por meio da degradação enzimática dos compostos orgânicos, de forma intracelular ou extracelular, sendo governada pela microbiota do solo (fungos, arqueias e bactérias) que ao final do processo excretam o N-NH4+ no solo.
A disponibilidade de N- NH4+ pelos microrganismos irá ocorrer em situações em que o material orgânico apresente estreita relação C/N.
- Nitrificação (NH4+—> NO2–—> NO3–)
O processo de nitrificação é a oxidação biológica do N amoniacal a nitrato, realizada no solo por bactérias quimioautotróficas, que obtém energia do processo e que podem sintetizar todos os seus constituintes celulares a partir do CO2.
O processo da nitrificação ocorre em dois passos sequenciais:
- Nitritação: a amônia é oxidada à nitrito através da ação bioquímica das bactérias como as do gênero Nitrossomonas.
Recentemente foi observado que bactérias do gênero Nitrospira também agem nesse processo, sendo estas encontradas principalmente em áreas agrícolas.
- Nitratação: ocorre a oxidação de nitrito para nitrato por ação de bactérias do gênero Nitrobacter.
Ambos os gêneros de bactérias somente desenvolvem atividade bioquímica na presença de oxigênio dissolvido, isto é, são aeróbios obrigatórios.
Quimicamente esses dois processos podem ser descritos como:
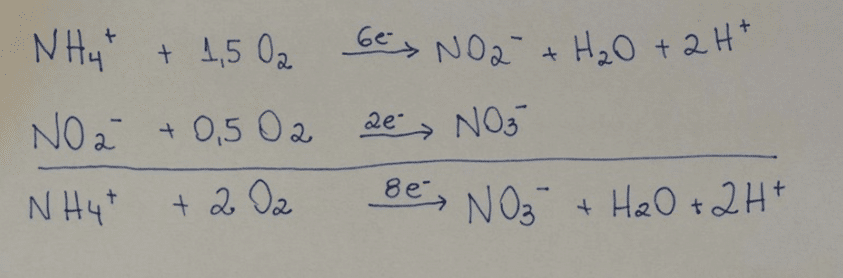
A reação de nitrificação libera dois mols de H+ para cada molécula de amônio oxidada o nitrato. Essa reação representa importante contribuição para a acidificação de solos agrícolas, especialmente aqueles adubados com fertilizantes nitrogenados amoniacais.
A taxa de nitrificação nos solos é influenciada por diversos fatores como:
- temperatura,
- umidade,
- quantidade de NH4+ presente solo,
- acidez do solo,
- presença e atividade dos microrganismos nitrificadores,
- uso de fertilizantes,
- relação C/N da MOS,
- presença de substâncias tóxicas
- presença e concentração de O2 (as bactérias responsáveis pelo processo de nitrificação não atuam em ambientes anaeróbios).
A adubação e a correção da acidez são práticas normais realizadas pelos agricultores no manejo de solos, que favorecem a atividade de microrganismos nitrificadores, acentuando a quantidade de NO3– no solo.
O predomínio de NO3– no solo é observado principalmente em sistemas com culturas anuais.
Tem sido relatado na literatura que algumas espécies de plantas forrageiras do gênero Brachiaria, como B. humidicola, B. decumbens, B. dictyoneura, e B. brizantha, liberam exsudados radiculares, denominados “braquiolatactanas” (metabólicos secundários) que exercem efeito inibitório sobre a nitrificação.
Isso porque, ao ser liberada no solo, a braquiolactana inibe a atividade da bactéria Nitrossomonas europea ocasionando a paralização das enzimas amônia mono-oxigenase e hidroxolamina oxiredutase, que são essenciais no processo de nitrificação.
Assim, talvez por estratégia adaptativa, nos solos cultivados com as referidas espécies de plantas forrageiras há um predomínio do íon NH4+ no solo em detrimento ao NO3–, diferente do que ocorre na maioria dos solos tropicais cultivados.
—
No processo de nitrificação, durante a oxidação de NH4+ a NO2–, pode haver pequena produção de óxido nitroso (N2O) por dismutação química do nitroxil (HNO) ou por ação da redutase do nitrito, conforme esquema a seguir:
NH4+ → NH2OH → [HNO] → NO2– → N2O
Embora o N2O normalmente seja produzido nos solos em condições anaeróbias pelo processo de desnitrificação, nesse caso, sua formação pode ocorrer em condições aeróbias, durante a nitrificação. Assim, este parece ser o principal meio como N2O é produzido em solos aeróbios com fertilizantes amoniacais.
Imobilização
A imobilização é um processo que ocorre concomitantemente com a mineralização, porém no sentido inverso. É a conversão do N-mineral (NH4+ e NO3–) em N-orgânico por microorganismos na decomposição de material orgânico com alta relação C/N.
Os microorganismos incorporam o N inorgânico disponível no solo em suas células, para conseguir decompor os resíduos vegetais que tem relação C/N alta (acima da ideal para os microorganismos).
Ao morrerem, o N assimilado pode voltar a ser mineralizado ou ser incorporados às células de outros microorganismos e seguir o caminho da síntese de compostos nitrogenados mais complexos, que gradualmente, formam a matéria orgânica do solo.
A assimilação de N inorgânico pelas plantas e a fixação de N2 da atmosfera por microorganismos do solo também representam imobilização do N inorgânico, mas são excluídas da definição de imobilização utilizada na ciclagem do N no solo.
Adição de material orgânico ao solo, tais como: restos de cultura, adubos verdes e orgânicos, afetam o equilíbrio entre mineralização e imobilização do solo.
A direção para onde os processos de mineralização-imobilização tende depende da relação C/Ndo material:
- Relação C/N de 20 a 31/1: mineralização ≈ imobilização (condição de equilíbrio);
- Relação C/N de 50 a 100/1: imobilização > mineralização;
Ocorre quando há adição de resíduos pobres em N, como resíduos de gramíneas ao solo: faz com que os microoganismos recorram ao N inorgânico disponível no solo para sustentar o crescimento da população, promovido pela abundância de C orgânico lábil. Com isso, a imobilização do N predomina.
Nessa fase as plantas apresentaram deficiência de N, visto que os microoganismos, numerosos e mais bem distribuídos no solo, competem com vantagem pelo N disponível.
À medida que o substrato é metabolizado, o C orgânico é oxidado e liberado na forma de CO2 no processo respiratório para gerar energia. Com isso a relação C/N diminui gradualmente até que os microorganismos não necessitem mais recorrer à utilização do N inorgânico do solo (C/N de 20 a 30/1).
Com a continuação do consumo do substrato, a relação C/N abaixa mais e passa a sobrar N no sistema, que é liberado (mineralizado). Resultados de literatura indicam que 2 a 3% do N orgânico do solo é mineralizado anualmente.
Os processos de mineralização-imobilização representam um subciclo dentro do ciclo do N no solo. A prevalência de um sobre o outro, ou seja, o resultado líquido de processos concorrentes, define se o solo terá maior ou menor disponibilidade de N inorgânico para as plantas.
Desnitrificação
A desnitrificação é um processo respiratório, que acontece na ausência de O2, no qual os óxidos são utilizados como receptores finais de elétrons.
É realizada por grande número de espécies de bactérias anaeróbias facultativas (principal grupos é das organotróficas), as quais na ausência de O2 utilizam o NO3– como receptor de elétrons.
A desnitrificação consome prótons e alcaliniza o meio, revertendo parte da acidez produzida durante a nitrificação.
O processo ocorre em quatro etapas, com reduções sucessivas do N. Os principais gases resultantes são o N2O e o N2, cujas proporções são variáveis de acordo com as condições do meio.
(+5) 2e- (+3) e- (+2) e- (+1) e- (0)
NO3– → NO2– → [NO] → N2O → N2
A desnitrificação também pode ser definida como a redução microbiana de NO3– a gases de N na forma molecular (N2) ou de óxidos (NO, N2O) em condições anaeróbicas. Contudo, vários tipos de metabolismo microbiano resultam na produção de N2O ou N2, inclusive a nitrificação, que ocorre em condições aeróbias.
A desnitrificação é influenciada pela (o):
- concentrações de nitrato e amônio do solo,
- conteúdo de água,
- disponibilidade de carbono,
- temperatura.
Embora somente ocorra em condições anaeróbias, solos em condições aeróbias também podem ter perdas gasosas por desnitrificação, visto que nesses solos há sítios anaeróbios. Em solos não saturados, porém, a disponibilidade de C frequentemente limita a desnitrificação.
Sistemas conservacionistas, que preservam palha ou restos vegetais sobre a superfície do solo são mais propensos às perdas por desnitrificação, uma vez que eles mantêm a umidade do solo por mais tempo e possuem fontes de carbono, como no sistema de cana-de-açúcar colhida sem queima.
A principal preocupação com a desnitrificação, além das perdas de N nos sistemas agrícolas é de cunho ambiental. O N2O é um gás importante para o efeito estufa e intermediário nas reações que resultam na destruição da camada de ozônio na estratosfera. Por isso há grande interesse em se conhecer as quantidades de N2O emitida do solo durante a desnitrificação, e as condições que favorecem tais emissões.
As perdas do N-fertilizante por desnitrificação nos sistemas agrícolas são extremamente variáveis e suas quantificações pouco precisas e exatas.
De modo geral, estima-se que variem de 5 a 30% do N aplicado como fertilizante. Essas estimativas provêm de estudos de balanço de N e englobam N não contabilizados, podendo ser perdido tanto na forma de desnitrificação como por volatilização.
Determinações diretas de perdas de N2O e N2 são complexas e envolvem medição de pequenas quantidades de gases nitrogenados volatilizado em atmosfera que contêm naturalmente 78% de N2 em sua composição, portanto são de difícil quantificação.
Perdas do ciclo do nitrogênio no sistema solo-planta
Lixiviação do nitrato
O ânion nitrato tem baixa interação química com os minerais do solo. A predominância de cargas negativas no solo, ou pelo menos nas camadas mais superficiais dos solos tropicais e a baixa interação química do nitrato com os minerais do solo faz com que ele esteja sujeito à lixiviação nas camadas mais profundas, podendo atingir águas superficiais ou o lençol freático.
A lixiviação do nitrato tem estreita dependência da quantidade de água que percola no perfil do solo.
A textura dos solos também afeta a lixiviação, que é maior em solos arenosos, que, por apresentarem menor microporosidade, tem movimentação mas rápida da água no sentido descendente.
O nitrato não é retido em solos com predominância de cargas eletronegativas, mas muitos solos tropicais têm horizontes subsuperficiais com cargas positivas que podem retardar consideravelmente a lixiviação do nitrato.
Embora haja poucos os trabalhos que avaliem as perdas do nitrato por lixiviação, estes consideram que as perdas no Brasil são baixas.
Os solos mais propensos às perdas por lixiviação são os que:
- recebem doses de N em excesso,
- solos revolvidos por aração e gradagem ou
- estão em períodos em que as plantas não absorvem grandes quantidades de N, como após a colheita, ou em estádios iniciais de crescimento.
Nesses casos a quantidade de nitrato no solo é maior e/ou não são requeridos nas mesmas proporções pelas plantas, o que pode causar sua perda por lixiviação.
O nitrato perdido por lixiviação pode atingir o lençol freático, e devido aos seus elevados teores nas águas causar a eutrofização, causando poluição ambiental.
Volatilização da amônia
A ação do homem é responsável por cerca de 75 % das emissões atmosféricas de N na forma de NH3 (que no total são estimadas em 54 Tg ano-1 ou 54 x 1012 g por ano).
A principal fonte de NH3 do mundo é a criação de animais e seus dejetos, em virtude das altas perdas de N da urina e das fezes por volatilização.
Também são relevantes as perdas oriundas da utilização de fertilizantes nitrogenados e da queima de vegetação. Maior ênfase será dada ao uso dos fertilizantes nitrogenados.
Dentre os fertilizantes nitrogenados a ureia é o mais utilizado no Brasil e no mundo e o que mais sofre com as perdas de volatilização, sendo este um dos principais fatores responsáveis pela baixa eficiência da ureia aplicada sobre a superfície do solo.
Quando aplicada no solo, a ureia passa por hidrolise da fonte nitrogenada e sofre ação da enzima urease, resultando na formação de carbonato de amônio, composto instável, que é desdobrado em NH3, CO2 e H2O.
Parte da NH3 formada reage com íons H+ da solução do solo e com íons H+ dissociáveis do complexo coloidal, resultando no cátion NH4+. Contudo, ao redor dos grânulos do fertilizante pode haver uma elevação do pH, que pode atingir valores de 7. Esses elevados valores de pH conduzem a volatilização da amônia, devido à baixa formação e íons NH4+.

A urease é uma enzima extracelular produzida por bactérias, actinomicetos e fungos do solo, ou ainda de origem dos restos culturais.
Fatores que tem influência sobre a urease, como pH, temperatura e umidade do solo afetam a hidrólise da ureia e volatilização de N-NH3.
Além disso, as trocas gasosas, taxa de evaporação de água, conteúdo de água no solo, teor de matéria orgânica, presença de cobertura vegetal, entre outros, também afetam a volatilização de amônia.
Assim, valores elevados de pH conduzem à maior volatilização de amônia da ureia aplicada em superfície, a qual pode representar até 80% do total de N aplicado, dependendo das condições climáticas e de solo.
As perdas de N-NH3 por volatilização podem ser cessadas com a incorporação da ureia ao solo, o que pode não ser viável em muitos sistemas de cultivo (seja pela presença de restos vegetais na superfície ou por questões de rendimento de cultivo e econômicas).
Outros manejos que visam reduzir a volatilização são a utilização de fertilizantes de eficiência aumentada (encapsulados, ou supergrânulo de ureia), a aplicação seguida de irrigação, etc.
Perdas de N pela parte aérea das plantas
As plantas podem tanto absorver NH3 do ar quanto perder NH3 para o ar devido a volatilização.
As principais perdas de amônia pela parte aérea das plantas ocorrem durante os estágios de crescimento reprodutivo, onde há intensa remobilização de N na planta.
Durante a senescência foliar o aumento da hidrólise de proteínas é acompanhado pela redução nas atividades das enzimas glutamina sintetase (GS) e glutamato sintase (GOGAT), principais responsáveis pela assimilação da amônia no metabolismo do N nas plantas superiores. A redução na atividade dessas enzimas resulta em perdas de NH3 na corrente transpiratória.
Essas perdas dependem do equilíbrio, em solução, entre a forma gasosa NH3 e a iônica NH4+, que é influenciado pela temperatura e pelo pH do meio.
A intensidade e o sentido com que ocorrem as trocas de amônia entre as folhas e a atmosfera dependem do ponto de compensação de amônia, que pode variar com a temperatura, intensidade luminosa e fotoperíodo, com a nutrição nitrogenada da planta, a espécie e a cultivar da mesma espécie, e o estágio vegetativo da planta.
Nas concentrações de NH3 na atmosfera abaixo do ponto de compensação de amônia da planta, ocorre sua emissão pelas folhas; em concentrações acima, sua absorção.
Conclusões
a compreensão das intricadas translocações e transformações no ciclo do nitrogênio é de suma importância para abordar desafios ambientais, agrícolas e relacionados à preservação dos recursos naturais.
As interações dinâmicas entre os processos de mineralização, imobilização, desnitrificação, lixiviação, volatilização e perdas pela parte aérea das plantas destacam a complexidade desse sistema solo-planta.
Fatores físicos, biológicos e climáticos desempenham papéis cruciais na regulação desses processos, influenciando diretamente a fertilidade do solo e a disponibilidade de nitrogênio para as culturas agrícolas.
Ao continuar a investigação nesse campo, podemos aprimorar práticas de manejo do solo e desenvolver estratégias sustentáveis para otimizar a eficiência do uso de nitrogênio, minimizando impactos ambientais e promovendo a produtividade agrícola.
—-
Se você quer receber gratuitamente no seu e-mail todo mês nosso informativo técnico que traz assuntos de maneira prática e objetiva, clique agora mesmo em “inscreva-se”.
Sobre a autora

Beatriz Nastaro Boschiero
Especialista em Conteúdo na Agroadvance
- Pós-doutora pelo CTBE/CNPEM e CENA/USP
- Mestra e Doutora em Solos e Nutrição de Plantas (ESALQ/USP)
- Engenheira Agrônoma (UNESP/Botucatu)







